Допомогою у визначенні валентності хімічного елемента є система елементів . Для прикладу валентність елементів I групи дорівнює I, а валентність елементів II групи дорівнює II. Хлор та інші метали 17 груп, які знаходяться останніми у формулі (наприклад, … Cl), мають валентність I.
Теорія:
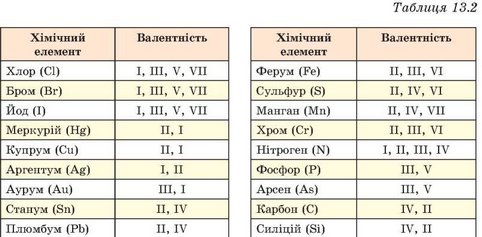
| Елемент | Валентність |
|---|---|
| S | II , IV , VI |
| Cl , Br , I | I , III , V , VII |
| Fe | II , III |
| Cu | I , II |
Щоб визначити валентність елемента за формулою бінарної сполуки, необхідно добуток величини валентності й індексу одного елемента поділити на індекс іншого.
Валентність хімічних елементів Наприклад, Гідроген, Натрій і Калій у своїх сполуках бувають тільки одновалентні, Кальцій, Барій, Магній, Цинк і Оксиген — тільки двовалентні, а Бор і Алюміній — тільки тривалентні.
Виняток — відносна атомна маса Хлору: A r ( Cl ) = 35,5. Відносна молекулярна маса M r — це відношення маси молекули або формульної одиниці до атомної одиниці маси.

Яку електронну формулу має хлор? Валентність пов ‘язана з особливостями зовнішнього енергетичного рівня, тому запишемо конфігурацію даного елемента. У неприйнятному стані на першому рівні у хлору розташовуються всього два електрони, другий займають вісім, на третьому …