Еквівалент речовини можна розрахувати з виразу Е=me/М, а число еквівалентів – з виразу ne = М/me. Наприклад, еквівалент сполуки (Е) Al2(SO4)3 = me(Al2(SO4)3)/М(Al2(SO4)3) =1/6, а число еквівалентів (ne) = me(Al2(SO4)3)/М(Al2(SO4)3) = 6.
Масу еквівалентну речовини можна розрахувати, як суму еквівалентних мас йонів. Наприклад: me(Al2(SO4)3) = me(Al3+) + me(SO42–) = 27/3 + 98/2 = 57 г/моль.
Експериментально для визначення еквівалентної маси металу необхідно наважку цього металу ввести в реакцію з надлишком кислоти. При цьому виділиться еквівалентна кількість водню. – еквівалентний об'єм водню, л/моль-екв. Об'єм водню, що виділиться при реакції, визначають експериментальним шляхом.
Закон еквівалентів — маси речовин, які вступають у реакцію та утворюються після неї, пропорційні молярним масам їхніх еквівалентів.
Еквівалент солі = Мr/ В . n (В – валентність металу; n – число атомів металу у солі) або дорівнює Мекв (металу) + Мекв (кислотного залишку).
Молярна маса еквівалента (Meq(B) або Е(В)) речовини В = M(B) / z(B). Аналітична хімія / В. В.

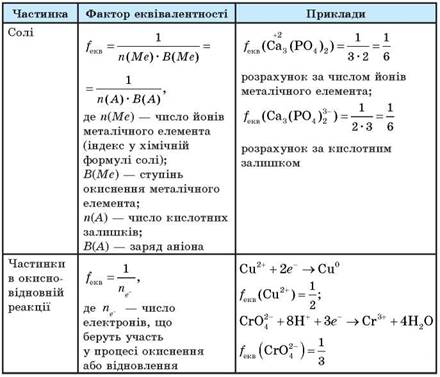
еквівалентні кількості речовини – завжди однакові в певній хімічній реакції. n eq = ν / f eq. Кількість еквівалентів речовини прийнято позначати як n eq моль еквівалент.