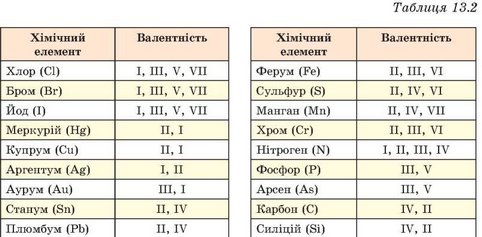
Допомогою у визначенні валентності хімічного елемента є система елементів . Для прикладу валентність елементів I групи дорівнює I, а валентність елементів II групи дорівнює II. Хлор та інші метали 17 груп, які знаходяться останніми у формулі (наприклад, … Cl), мають валентність I.
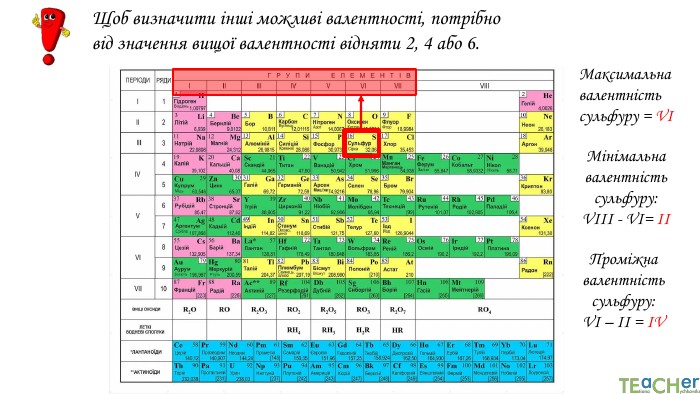
Максимальна валентність елемента дорівнює номеру групи, мінімальна – для неметалів дорівнює різниці числа 8 і номеру групи, у якій стоїть елемент.
Теорія:
| Елемент | Валентність |
|---|---|
| H , F , Li , Na , K , Ag | I |
| O , Be , Mg , Ca , Ba , Zn | II |
| Al | III |
Валентність елементів можна визначати за допомогою Періодичної системи елементів. Номер групи, в якій міститься елемент показує максимальну валентність елемента. Майже всі елементи I, II, III груп ПС проявляють сталу валентність.
Виняток — відносна атомна маса Хлору: A r ( Cl ) = 35,5. Відносна молекулярна маса M r — це відношення маси молекули або формульної одиниці до атомної одиниці маси.
валентність o = ii (ступінь окислення -2). Тоді: 1 + х – 2 * 4 = 0, звідси х = 7. Аналогічним чином можна порахувати валентність хлору в інших з’єднаннях